Vào ngày 5 tháng 7, Novo Nordisk đã triển khai thử nghiệm lâm sàng giai đoạn III đối với thuốc tiêm CagriSema ở Trung Quốc, mục đích là so sánh tính an toàn và hiệu quả của việc tiêm CagriSema với semeglutide ở bệnh nhân béo phì và thừa cân ở Trung Quốc.
Thuốc tiêm CagriSema là một liệu pháp phối hợp tác dụng kéo dài đang được Novo Nordisk phát triển, thành phần chính là chất chủ vận thụ thể GLP-1 (glucagon-like peptide-1) smeglutide và cagrilintide tương tự amylin tác dụng kéo dài.Thuốc tiêm CagriSema có thể được tiêm dưới da mỗi tuần một lần.
Mục tiêu chính là so sánh CagriSema (2,4 mg/2,4 mg) với semeglutide hoặc giả dược tiêm dưới da một lần mỗi tuần.Novo Nordisk vừa công bố kết quả thử nghiệm CagriSema trong điều trị bệnh tiểu đường giai đoạn 2, chứng minh tác dụng hạ đường huyết của CagriSema tốt hơn semeglutide và gần 90% đối tượng đã đạt được mục tiêu HbA1c.
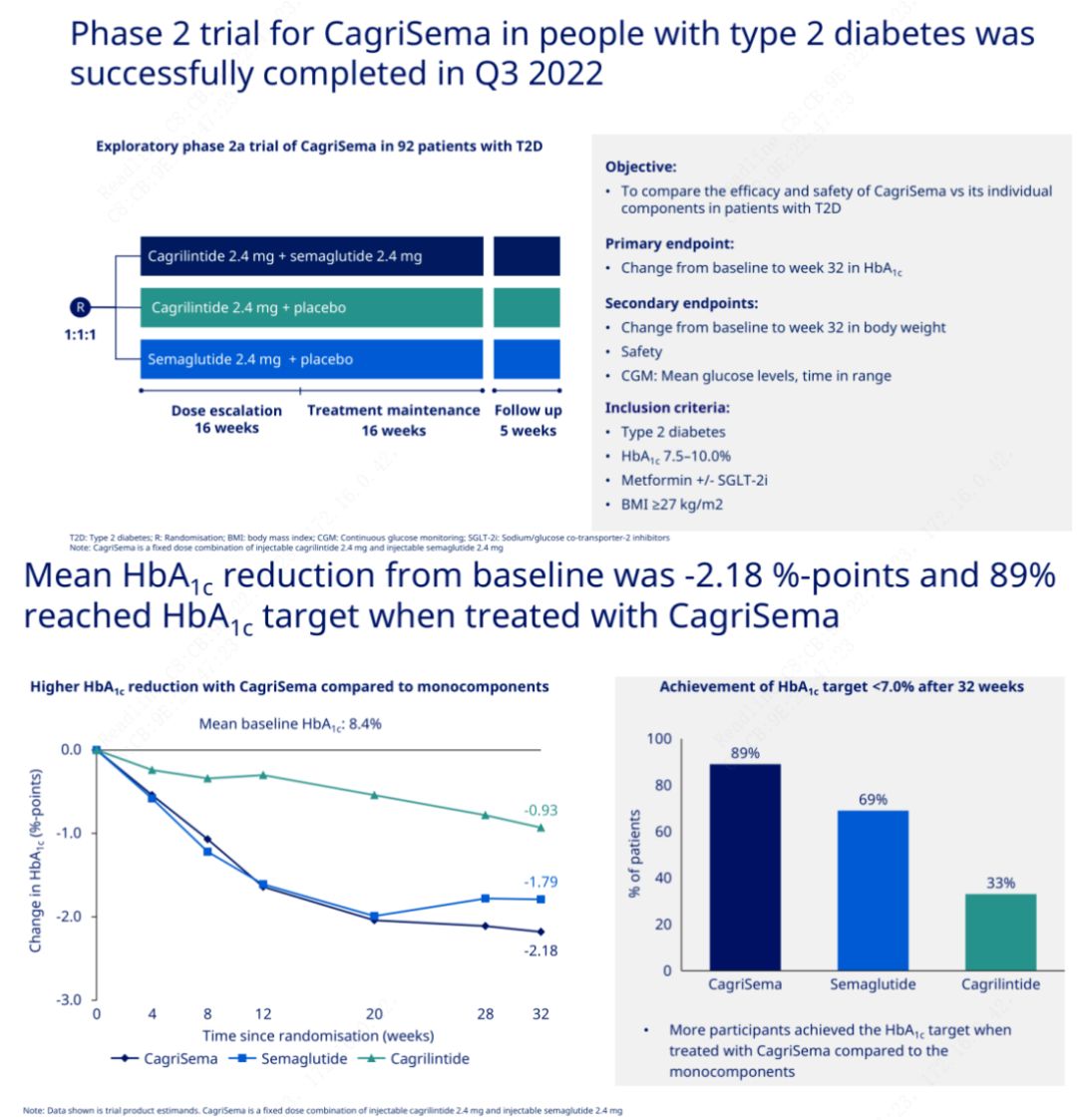
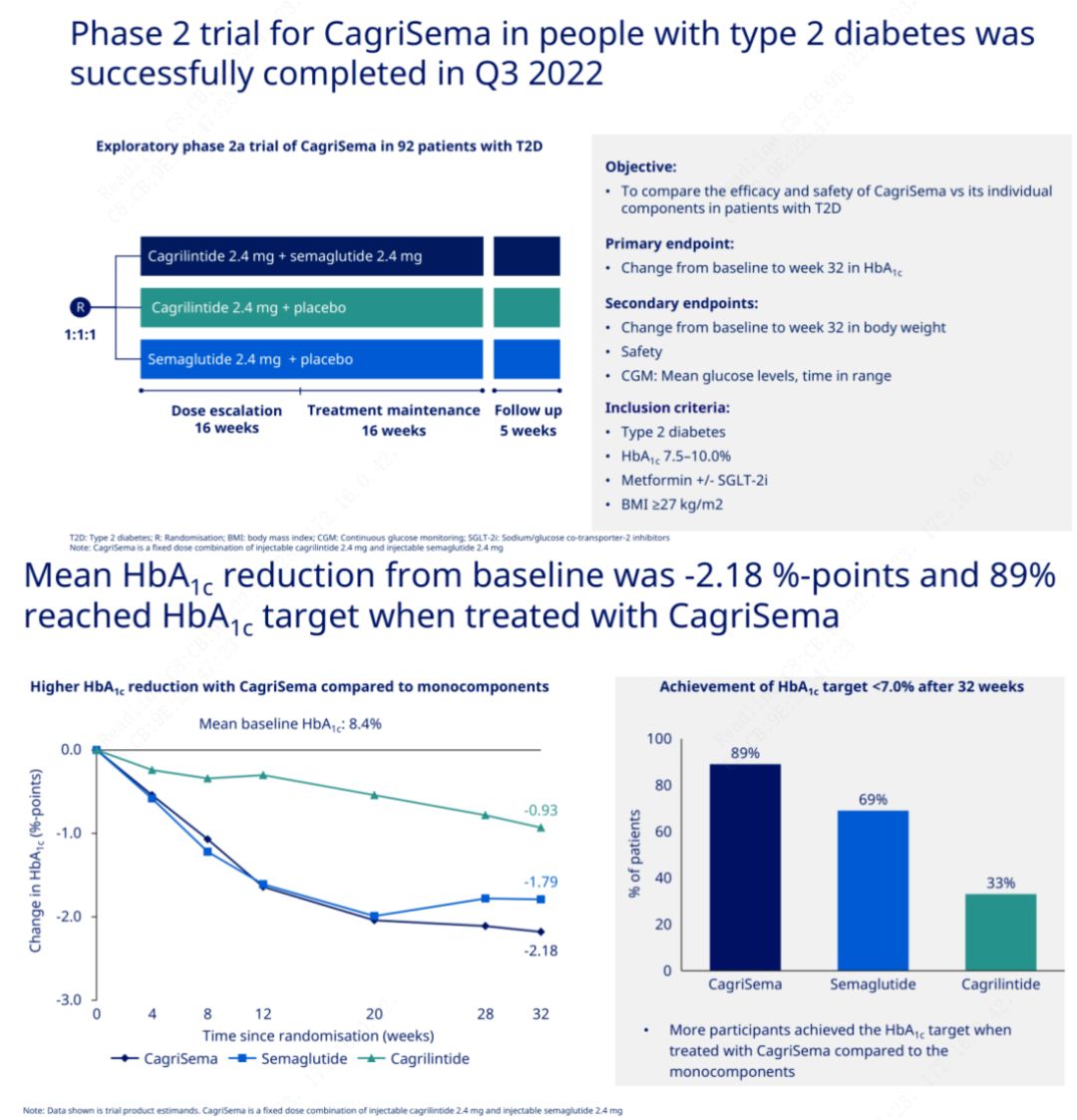
Dữ liệu cho thấy ngoài tác dụng hạ đường huyết đáng kể, về mặt giảm cân, thuốc tiêm CagriSema vượt trội đáng kể so với semeglutide (5,1%) và cagrilintide (8,1%) với mức giảm cân là 15,6%.
Thuốc cải tiến Tirzepatide là thuốc chủ vận thụ thể GIP/GLP-1 hàng tuần được phê duyệt đầu tiên trên thế giới.Nó kết hợp tác dụng của hai incretin thành một phân tử duy nhất được tiêm mỗi tuần một lần và là một phương pháp điều trị mới cho bệnh tiểu đường loại 2.Tirzepatide đã được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phê duyệt vào tháng 5 năm 2022 để cải thiện việc kiểm soát đường huyết (dựa trên chế độ ăn kiêng và tập thể dục) ở người lớn mắc bệnh tiểu đường loại 2 và hiện đang được phê duyệt ở Liên minh Châu Âu, Nhật Bản và các quốc gia khác.
Vào ngày 5 tháng 7, Eli Lilly đã công bố nghiên cứu SURPASS-CN-MONO giai đoạn III trên nền tảng đăng ký thử nghiệm lâm sàng thuốc và công bố thông tin để điều trị bệnh nhân tiểu đường loại 2.SURPASS-CN-MONO là nghiên cứu giai đoạn III ngẫu nhiên, mù đôi, đối chứng giả dược được thiết kế để đánh giá hiệu quả và độ an toàn của đơn trị liệu bằng tirzepatide so với giả dược ở những người mắc bệnh tiểu đường loại 2.Nghiên cứu dự kiến bao gồm 200 bệnh nhân mắc bệnh tiểu đường loại 2 không dùng bất kỳ loại thuốc trị đái tháo đường nào trong 90 ngày trước Lần khám 1 (ngoại trừ trong một số tình huống lâm sàng nhất định, chẳng hạn như bệnh cấp tính, nhập viện hoặc phẫu thuật tự chọn, thời gian ngắn (<14). ngày) sử dụng insulin).
Bệnh tiểu đường loại 2 dự kiến sẽ được phê duyệt trong năm nay
Tháng trước, kết quả của nghiên cứu SURPASS-AP-Combo đã được công bố ngày 25 tháng 5 trên tạp chí bom tấn Nature Medicine.Kết quả cho thấy so với insulin glargine, Tirzepatide cho thấy HbA1c và giảm cân tốt hơn ở nhóm bệnh nhân tiểu đường tuýp 2 ở khu vực Châu Á - Thái Bình Dương (chủ yếu là Trung Quốc): Giảm HbA1c tới 2,49% và giảm cân tới 7,2 kg. (9,4%) sau 40 tuần điều trị, cải thiện đáng kể lipid máu và huyết áp, độ an toàn và khả năng dung nạp nói chung là tốt.
Thử nghiệm lâm sàng Giai đoạn 3 của SURPASS-AP-Combo là nghiên cứu đầu tiên của Tirzepatide được thực hiện chủ yếu ở những bệnh nhân Trung Quốc mắc bệnh tiểu đường loại 2, do Giáo sư Ji Linong của Bệnh viện Nhân dân Đại học Bắc Kinh dẫn đầu.SURPASS-AP-Combo phù hợp với kết quả của loạt nghiên cứu SURPASS toàn cầu, điều này càng chứng minh rằng sinh lý bệnh của bệnh tiểu đường ở bệnh nhân Trung Quốc phù hợp với bệnh nhân toàn cầu, là cơ sở cho việc nghiên cứu và phát triển đồng thời các loại thuốc mới ở Trung Quốc và thế giới, đồng thời cung cấp bằng chứng hỗ trợ vững chắc về việc giúp bệnh nhân Trung Quốc có cơ hội sử dụng các loại thuốc điều trị bệnh tiểu đường mới nhất và ứng dụng lâm sàng của chúng ở Trung Quốc càng sớm càng tốt.
Thời gian đăng: 18-09-2023

